Lors de la cérémonie d’ouverture du Pasteur Network Annual Meeting, le 21 octobre 2024 à Rio de Janeiro, le Dr. Claire Sangba-Kembi-Ngounou, entomologiste à l’Institut Pasteur de Bangui (République centrafricaine), reçoit le Talent Award. Cette distinction, financée depuis 2017 par l’Institut Pasteur, met en lumière des jeunes chercheurs du Pasteur Network ayant démontré un potentiel scientifique. Pour la première fois, le prix s’inscrit dans la catégorie Science & Communication, reconnaissant la capacité des chercheurs à diffuser leurs travaux au grand public.
Un parcours au service de la santé publique
Claire Sangba-Kembi-Ngounou rejoint le département d’entomologie médicale de l’Institut Pasteur de Bangui afin de commencer sa thèse en 2015. Aujourd’hui, elle est une chercheuse montante en entomologie, ayant réussi à obtenir des financements de la Fondation Gates et du Wellcome Trust pour soutenir ses projets novateurs. Elle joue un rôle clé dans la lutte contre le paludisme en étudiant le comportement des moustiques, notamment les espèces Anopheles, vecteurs majeurs de la maladie. Son travail se concentre sur l’analyse de la diversité génétique et de l’adaptabilité des vecteurs du paludisme, avec des implications directes pour le contrôle de la maladie en République Centrafricaine. En comprenant les bases génétiques du comportement des moustiques et de leur résistance, ses recherches contribuent au développement de stratégies de lutte contre les vecteurs plus efficaces. Cela pourrait réduire les taux de transmission du paludisme et améliorer les résultats en matière de santé publique. Ses découvertes ont été publiées dans des revues scientifiques de premier plan, telles que le Proceedings of the National Academy of Sciences (PNAS).
Un pont entre la science et l’action publique
En plus de ses activités scientifiques, le Dr. Sangba-Kembi est fortement impliquée dans la diffusion de ces résultats à tous les échelons de la société ce qui lui a valu un article dédié dans le journal Le Monde, dans la série « En Afrique, la science au féminin ». Elle a des échanges réguliers avec le ministère de la Santé de la République Centrafricaine sur le développement de politique afin de limiter la transmission du paludisme. Elle utilisera une partie du financement de ce prix pour organiser une campagne de sensibilisation dans les écoles sur les changements dans le comportement de piqûre des moustiques et leurs implications pour la lutte contre le paludisme.
Valoriser la communication scientifique
Cette 8e édition du Talent Award est la première à récompenser un scientifique ayant non seulement un engagement scientifique fort, mais également une aptitude remarquable à communiquer ses recherches à un public plus large. Ce prix soutient des initiatives qui favorisent une communication claire et ouverte, essentielle pour instaurer la confiance entre la science et la société. En période de crise, comme lors des pandémies, une communication scientifique efficace influence directement le comportement et la sécurité du public.
“Encourager l’impact scientifique et la communication”
En félicitant le Dr. Claire Sangba-Kembi-Ngounou, Odette Tomescu Hatto, vice-présidente des affaires internationales à l’Institut Pasteur, souligne : « Le Talent Award célèbre aujourd’hui une scientifique qui incarne non seulement l’excellence scientifique, mais aussi la capacité de traduire ses recherches en actions concrètes, accessibles à tous. Le Dr. Sangba-Kembi-Ngounou démontre que la communication scientifique est un levier puissant pour façonner l’avenir de la santé publique. »
En tout, douze chercheurs ont déjà reçu ce prix depuis sa création. Le Talent Award 2024 marque un tournant en affirmant que la communication est un pilier indispensable pour maximiser l’impact de la recherche scientifique sur la société.
Pour en savoir plus : visionnez le replay de la cérémonie d’ouverture : https://www.youtube.com/live/4nvcIrt6IlQ
A propos du PNAM2024 : https://pasteur-network.org/news/actualites/la-reunion-annuelle-du-pasteur-network-2024-se-tiendra-a-rio-de-janeiro-bresil/
La Réunion Annuelle du Pasteur Network 2024 (PNAM), co-organisée avec la Fondation Oswaldo Cruz (Fiocruz), se tiendra du 21 au 23 octobre dans la vibrante ville de Rio de Janeiro, au Brésil. Cet événement prestigieux rassemblera des leaders et des experts du Pasteur Network et au-delà, offrant une plateforme pour aborder les défis mondiaux les plus pressants en matière de santé. Les participants participeront à un riche programme de présentations, d’ateliers et de discussions visant à favoriser la collaboration et à stimuler l’innovation scientifique. Avec un accent sur des sujets clés tels que la préparation aux épidémies, les maladies sensibles au climat et l’équité dans la recherche en santé, le PNAM 2024 promet d’être un catalyseur pour faire progresser les solutions de santé publique dans le monde entier.
La réunion abordera les priorités mondiales de santé, y compris le changement climatique et son impact sur les maladies infectieuses comme la Dengue, la préparation aux épidémies avec Mpox et la grippe aviaire, ainsi que les innovations en matière de diagnostics, l’équité d’accès aux vaccins, les traitements, la santé des femmes et des mères, et le rôle de l’intelligence artificielle dans la recherche en santé. Ces discussions s’alignent sur la vision stratégique du Pasteur Network visant à renforcer l’intelligence épidémique, promouvoir des collaborations équitables et encourager le développement durable dans la recherche en santé mondiale.
Cérémonie d’ouverture
La cérémonie d’ouverture aura lieu le lundi 21 octobre à 18h (heure de Rio de Janeiro UTC-3) et sera présidée par Mario Moreira, Président de la Fiocruz. Elle comportera des interventions de hauts responsables brésiliens, dont Nisia Veronica Trindade Lima, ministre de la Santé du Brésil. Amadou Sall, Président du Pasteur Network et Administrateur général de l’Institut Pasteur de Dakar, Rebecca Grais, directrice exécutive du Pasteur Network, et Yasmine Belkaid, vice-présidente du Pasteur Network et présidente de l’Institut Pasteur, prendront également la parole lors de la cérémonie d’ouverture.
Des allocutions seront données par des leaders mondiaux de la santé, notamment Peter Piot, professeur à la London School of Hygiene & Tropical Medicine et président du Conseil stratégique du Pasteur Network, ainsi que Manoel Barral Netto de Fiocruz Bahia, qui partageront leurs perspectives sur des enjeux de santé mondiale cruciaux.
À 19h15, la cérémonie des Talent Awards aura lieu, célébrant les contributions exceptionnelles au sein du Pasteur Network. Cette année, le prix, financé par l’Institut Pasteur, récompensera un(e) scientifique ayant démontré à la fois son excellence scientifique et un fort engagement à partager ses travaux avec le grand public à travers des initiatives de communication et d’engagement.
Suivez la diffusion en direct
La cérémonie d’ouverture sera diffusée en direct sur YouTube :
Engagement et discussions stratégiques
Tout au long de l’événement, les participants prendront part à une série de tables rondes et de sessions parallèles axées sur les priorités stratégiques du Pasteur Network : (1) Veiller et se prépararer aux épidémies, avec un accent sur les maladies sensibles au climat ; (2) Faire avancer la recherche, le développement et l’innovation ; (3) construire des communautés de partage de connaissances ; et (4) promouvoir des collaborations équitables et durables.
La réunion offrira également une plateforme aux scientifiques du Réseau pour présenter leurs recherches, contribuant ainsi à l’objectif de développement professionnel de la PNAM.
Pour plus de détails sur l’événement :
A propos du Pasteur Network
Le Pasteur Network est une alliance de plus de 30 instituts qui joue un rôle essentiel dans la réponse aux défis de santé mondiaux par la science, l’innovation et la santé publique. Le réseau se distingue par sa diversité et sa large couverture géographique, qui s’étend sur 25 pays sur les 5 continents, favorisant une communauté dynamique de connaissances et d’expertises.
Le Pasteur Network est reconnu comme un acteur non-étatique de l’OMS et ses membres sont souvent dépendants des ministères de la santé locaux. Il dispose d’une infrastructure mondiale comprenant plus de 50 laboratoires de référence nationaux et régionaux, dont de nombreux laboratoires de niveau 3 de biosécurité, et 17 Centres Collaborateurs de l’OMS. Les activités du Pasteur Network sont guidées par quatre piliers stratégiques : 1) la veille et préparation aux épidémies, avec un accent sur les maladies sensibles au Climat, 2) la recherche, le développement et l’innovation, 3) les communautés de connaissances, et 4) la gouvernance et l’équité.
Pour en savoir plus, consulter le rapport 2023 du Pasteur Network
Contact presse : Juliette Hardy / news-pn@pasteur.fr
À propos de la Fiocruz
Fiocruz est la plus grande institution de recherche biomédicale en Amérique latine, produisant également des vaccins et des médicaments pour approvisionner le Système de Santé Unifié (SUS). Liée au ministère de la Santé, elle a été fondée le 25 mai 1900, initialement pour fabriquer des sérums et des vaccins contre la peste bubonique. Depuis, l’institution a suivi une trajectoire marquée par le développement de la santé publique au Brésil. Aujourd’hui, Fiocruz est présente dans 10 États ainsi que dans le District fédéral, et possède un bureau à Maputo, la capitale du Mozambique, en Afrique. En plus de ses instituts basés à Rio de Janeiro, elle maintient des unités dans les régions Nord-Est, Nord, Sud-Est et Sud du Brésil. Au total, elle compte 16 unités technico-scientifiques consacrées à l’éducation, à la recherche, à l’innovation, à l’assistance, au développement technologique et à la diffusion dans le secteur de la santé. Pour plus d’informations, visitez https://portal.fiocruz.br/en
Contact presse : ccs@fiocruz.br
Les 13 et 14 août 2024, le CDC Afrique et l’OMS ont déclaré que Mpox était une urgence de santé publique de portée internationale (PHEIC).
Dans le cadre de son engagement permanent en faveur de la science, de l’innovation et de la santé publique mondiale, le Réseau Pasteur, réputé pour son expertise dans le domaine des maladies infectieuses et sa vaste portée géographique, couvrant 25 pays sur les 5 continents, intensifie ses efforts pour lutter contre l’épidémie de Mpox en cours.
S’appuyant sur cette alliance mondiale de plus de 30 instituts, nos équipes multidisciplinaires sont à la pointe de la recherche et des efforts de réponse à ce défi de santé publique, travaillant sans relâche pour renforcer la surveillance, améliorer les diagnostics et soutenir le développement d’un accès équitable aux traitements.
Parmi les membres du réseau Pasteur, plusieurs instituts ont développé une expertise dans la surveillance, le diagnostic et la recherche sur le Mpox au cours des précédentes épidémies dans la région.
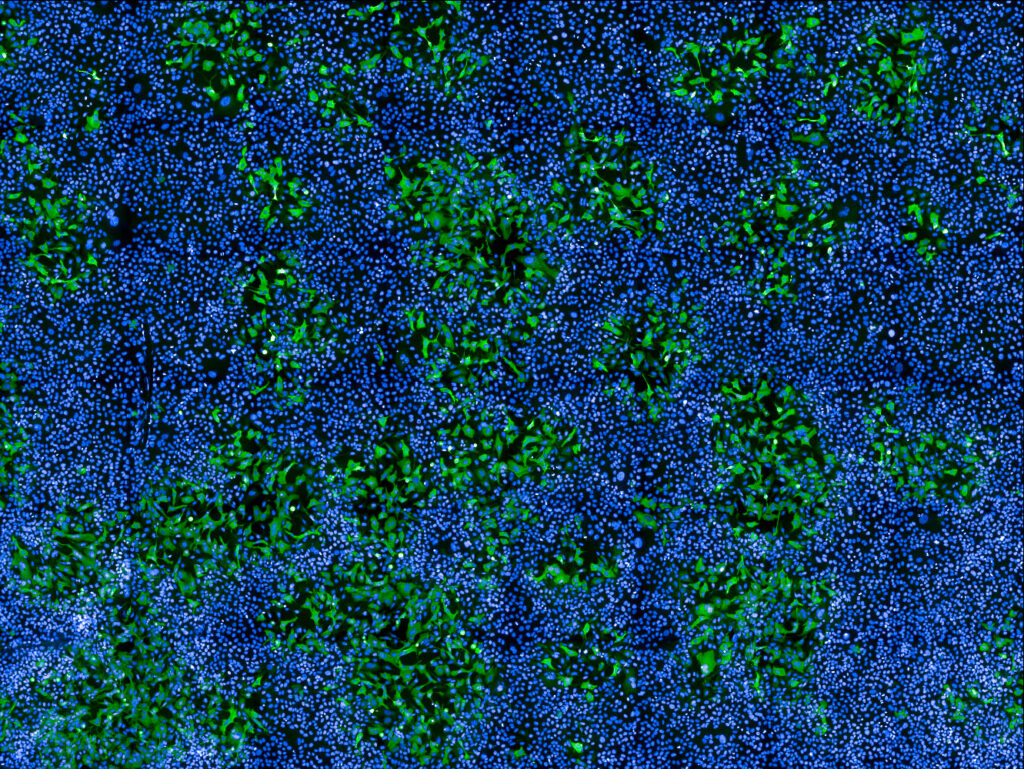
Cellules humaines infectées par MPXV (en vert) parmi des cellules non infectées (noyaux en bleu). Image prise au microscope confocal. Copyright : Institut Pasteur/Mathieu Hubert et Olivier Schwartz
Les membres du réseau Pasteur développent des actions dans de nombreux domaines :
Surveillance et diagnostic
- Contribuer à la surveillance, en particulier dans les régions à forte transmission, grâce à des capacités de diagnostic et à la formation.
Recherche et développement
Tirer parti d’une vaste expertise en virologie pour détecter et comprendre la dynamique de la transmission et soutenir le développement de contre-mesures médicales.
Collaboration
- Soutenir l’accès équitable aux solutions ciblant les populations à haut risque, en coordination avec les autorités sanitaires locales, comme le prévoit la déclaration de Rio signée par le réseau Pasteur.
- Etablir des partenariats avec des organisations de santé mondiale afin d’aider à traduire la recherche en politiques et en solutions concrètes.
Alors que le monde est confronté à de nouveaux défis, le réseau Pasteur reste attaché à l’excellence scientifique et à la collaboration, ce qui nous permet de répondre aux besoins émergents en matière de santé publique.
L’enseignement et la formation constituent une part essentielle du travail des membres du Pasteur Network. Les cours internationaux du Network répondent aux priorités de la recherche et de la santé publique aux niveaux mondial et régional, en offrant une formation de haut niveau à des scientifiques à différents stades de leur carrière et en renforçant les relations scientifiques entre les scientifiques au sein du réseau et avec d’autres institutions.
Les candidatures sont ouvertes pour les membres du réseau Pasteur
Depuis 2012, le Pasteur Network a proposé plus d’une centaine de cours théoriques et pratiques dans le monde entier. Les cours internationaux et les ateliers de formation ont trois objectifs principaux :
- Répondre aux priorités mondiales et régionales en matière de recherche et de santé publique.
- Offrir une formation de haute qualité à des scientifiques à différents stades de leur carrière.
- Renforcer les relations scientifiques entre les chercheurs au sein du Pasteur Network et avec d’autres institutions.
En accord avec la mission du Pasteur Network, les cours et ateliers de formation sont ouverts aux étudiants post-universitaires et aux jeunes scientifiques du réseau ainsi qu’à toute autre institution de recherche (universités, agences de santé publique, organisations gouvernementales, etc.) du pays hôte et des institutions nationales.
DIRECTIVES POUR LES COURS
Pour une candidature réussie, nous vous encourageons à lire attentivement les directives suivantes.
Étapes de candidature
Soumission des propositions, date limite : 15 novembre 2024
Les candidats sont invités à soumettre leur cours en ligne sur Flexigrant. Suivez ce lien : https://calls.pasteur-network.org/startapplication.aspx?id=13738
Évaluation par le comité de sélection, date limite : décembre 2024
Les propositions seront examinées par un comité interne d’experts.
Communication des résultats : décembre 2024

Critères de sélection
Pour être sélectionnés, les cours doivent répondre aux critères suivants :
- Qualité : Le cours doit être correctement organisé et couvrir des sujets pertinents et de haute qualité. L’équipe d’enseignants/instructeurs doit être expérimentée et compétente dans le domaine. Un plan clair de suivi et d’évaluation doit être défini et les objectifs d’apprentissage doivent être énumérés.
- Pertinence : Seuls les cours qui s’inscrivent dans les axes stratégiques prioritaires du Pasteur Network seront pris en compte. Ces axes incluent i) le renforcement de la préparation aux épidémies ainsi que la Santé et le Climat, ii) la recherche, le développement et l’innovation dans les diagnostics, vaccins et thérapeutiques, iii) la création de communautés de connaissances pluridisciplinaires, et iv) la promotion de la collaboration équitable. Tous les sujets scientifiques sont éligibles dans ces axes stratégiques, bien que la priorité soit donnée à ceux énumérés dans la stratégie scientifique du Pasteur Network.
- Préférence pour les instituts du réseau : La priorité sera accordée aux cours organisés au sein et par un institut membre du Pasteur Network.
- Institutions partenaires : La priorité sera accordée aux cours associant des institutions partenaires.
- Implication des formateurs/intervenants locaux : Les formateurs/intervenants locaux doivent être impliqués dans le cours.
- Public cible : Le cours doit s’adresser aux scientifiques, ingénieurs et techniciens seniors. La priorité sera donnée aux candidats du Pasteur Network (au moins 50 %) et aux candidats externes, tous sélectionnés en fonction de leurs mérites.
- Outils éducatifs innovants : L’utilisation d’outils éducatifs innovants est fortement encouragée et sera vue positivement lors du processus de sélection. Des outils en ligne ou numériques peuvent être utilisés pour améliorer l’expérience du cours (réalité virtuelle augmentée, gamification/ludification, systèmes collaboratifs de gestion de l’apprentissage (LMS), etc.).
- Calendrier : Le cours doit être terminé avant le 20 décembre 2025.
- Soutien financier maximal : 50 000 €
Critères de financement
- Le financement du cours doit être justifié et en ligne avec le format soumis.
- Le Pasteur Network financera un maximum de 80 % du budget total du cours. Les candidats sont encouragés à compléter leur budget par un financement externe.
Paiement des fonds
- 85 % du financement attribué sera transféré par virement bancaire à l’institut organisateur, après réception de la facture, 3 à 4 mois avant le cours.
- 15 % seront transférés après réception du rapport complet du cours (voir section rapport du cours).
Dépenses éligibles
Les dépenses éligibles pour le financement sont :
- Consommables
- Frais de déplacement
- Coûts du logement
- Restauration
- Frais de communication
- Coûts de transport local
Dépenses non éligibles
Les dépenses non éligibles pour le financement sont :
- Frais généraux ou coûts indirects
- Paiements aux enseignants/instructeurs et aux étudiants (y compris per diem)
- Équipement
- Location (de locaux) dans un institut du Réseau
Par « dépenses non éligibles », nous entendons que les éléments cités ne seront pas considérés comme des dépenses directes sur le financement du Pasteur Network. La participation en nature de l’institut récepteur peut être valorisée comme cofinancement. En cas de doute ou de question sur d’autres coûts directs, le Pasteur Network doit être contacté pour clarification.
Rapport de cours
Un rapport technique et financier devra être envoyé un mois après la fin du cours.
Le transfert des 15 % restants des fonds attribués par le Pasteur Network est soumis à la réception du rapport complet.
Remboursement
Dans le cas où les fonds attribués par le Pasteur Network n’ont pas été utilisés, les fonds restants devront être remboursés au Pasteur Network.
Contact
Pour toute question, veuillez contacter Renaud Vatrinet à l’adresse renaud.vatrinet@pasteur.fr.
Lancement du programme d’Observatoires Climat-Santé au sein du Pasteur Network lors de la réunion sur le Climat-Santé à Dakar, les 4-5 juin 2024
Le 4 et 5 juin à Dakar au Sénégal, plus de 60 participants, membres du Pasteur Network (PN) et experts externes, se sont réunis pour discuter de la façon dont le Pasteur Network peut aider à répondre à l’impact croissant du changement climatique sur la santé globale. L’objectif est de favoriser des recherches collaboratives et des solutions innovantes pour atténuer les menaces émergentes pour la santé et améliorer la résilience des systèmes de santé publique. L’événement a été soutenu par la Fondation Rockefeller et l’Institut de Philanthropie, qui financent le programme d’Observatoires Climat-Santé du Pasteur Network.
Celui-ci vise à :
- Créer les bases des observatoires Climat-Santé en créant un réseau global de boursiers.
Ce programme de bourse est une opportunité unique conçue pour les membres des pays à faible et moyen revenu (LMIC) pour équiper les chercheurs pour les aider à fournir un soutien aux acteurs locaux dans les prises de décisions éclairées concernant le climat et la santé. - Développer des outils et des pratiques généralisables en utilisant des exemples au sein du Pasteur Network.
Les membres-exemples du Pasteur Network partageront leur connaissance et leur expertise en matière de climat et de santé et aideront à coordonner le réseau de boursiers dans leur région. - Augmenter l’impact grâce au partage des connaissances via Global Goods (biens mondiaux) Get une plateforme interne de partage des connaissances. L’événement de Dakar a vu l’organisation de sessions de discussion en petits groupes portant spécifiquement sur la conception du programme de bourses et le développement de produits globaux.
Des experts mondiaux ont également présenté et animé des discussions sur divers sujets, tels que des mises à jour sur l’état d’avancement du traité sur les pandémies (Dr. Maria de Lourdes Aguiar Oliveira de FioCruz), les tendances importantes et les considérations pour intégrer les aspects climatiques dans les efforts de surveillance de la santé (Dr. Linda Venczel de PATH), l’établissement d’un lien entre les recommandations en matière de santé climatique et les décisions politiques et d’investissement prises par les parties prenantes gouvernementales (Mr. Jackson Kimani de Climate Action Platform for Africa-CAP-A), la présentation de la plateforme de collaboration HIVE de l’OMS (Mr. Brian Yau de l’OMS), et une table ronde sur le développement et la diffusion des global goods (biens mondiaaux) (Dr. Cristina Tato de Chan Zuckerberg Biohub, Mr. Gaurav Godhwani de Civic Data Lab, et Dr. Felipe Colón-González de Wellcome Trust).
La réunion a également été l’occasion de contribuer à la célébration du 100e anniversaire de l’Institut Pasteur de Dakar, incluant une visite de l’Institut de l’institut et un cocktail.
Le 100e anniversaire de Dakar marque un siècle de recherche pionnière, d’innovation et de contributions à la santé mondiale, renforçant son rôle vital dans la lutte contre les maladies infectieuses et l’amélioration de la santé publique dans le monde entier. Le Pasteur Network exprime ses remerciements les plus sincères à la Fondation Rockefeller et à l’Institut de Philanthropie pour leur généreuse aide, qui a rendu possible la réunion à Dakar les 4 et 5 juin. Nous remercions également tous les participants pour leurs contributions précieuses et leur engagement, qui ont été essentiels pour nos discussions sur l’intersection critique du climat et de la santé.










Six jeunes diplômés issus des membres du Pasteur Network ont été mis à l’honneur lors de la Cérémonie de remise des diplômes de doctorants de l’Institut Pasteur le 8 décembre 2023. Cette célébration a marqué la fin d’un chapitre pour cette nouvelle génération de chercheurs et a mis en lumière l’excellence de la communauté scientifique formée à l’Institut Pasteur, membre du Pasteur Network.
Organisée par le Département de l’Enseignement depuis 2013, cette célébration a marqué son 11e anniversaire en soulignant la qualité scientifique des jeunes diplômés qui ont été en partie formés à l’Institut Pasteur.
Présidée par Monical Sala, Directrice de l’Enseignement à l’Institut Pasteur et Vincenzo di Bartolo, cette édition a introduite par Valérie Masson-Delmotte, climatologue, directrice de recherche au CEA et co-présidente du groupe de travail 1 du Groupe d’experts intergouvernemental sur l’évolution du climat (GIEC), en tant qu’invitée d’honneur.
Valérie Masson-Delmotte a présenté le lien intrinsèque entre le changement climatique et la recherche en soulignant comment l’augmentation de la température favorise la propagation des maladies à transmission vectorielle. Il est donc essentiel de poursuivre la recherche pour apporter une réponse active à cette question urgente.
Les diplômés ont ensuite été présentés par Monica Sala et Rebecca Grais, Directrice Exécutive du Pasteur Network.
Les doctorants viennent des quatre régions du Pasteur Network – Afrique, Amériques, Asie-Pacifique, Euro-méditerranée – et ont eu l’occasion de travailler sur une grande variété de sujets décrits ci-dessous. Ils ont choisi de partager une citation qui les inspire.
- Elliot Fara Nandrasana RAKOTOMANANA

Doctorat en anthropologie sociale et culturelle, université de Bordeaux (France)
Institut Pasteur de Madagascar /unité d’épidémiologie et de recherche clinique
Thèse : « Stunting and the risk of contamination by the living environment. An anthropology of early childhood through the prism of spatial and social organizations in a disadvantaged neighborhood in Antananarivo » (Madagascar)
« Ne rien lâcher ! La passion, le courage et la détermination nous permettent de surmonter la peur, la tristesse… le progrès et les obstacles à la réussite. »
Elliot Rakotomanana décroche un DEA en biochimie appliquée à la nutrition à l’université d’Antananarivo (Madagascar) en 2006. En 2014, il rejoint l’unité d’épidémiologie et de recherche clinique de l’Institut Pasteur de Madagascar (IPM) en tant que coordinateur national d’une étude socio-anthropologique sur le retard de croissance. Passionné d’anthropologie, il poursuit des études dans cette discipline à l’université de Bordeaux à partir de 2016, dans le cadre du projet AFRIBIOTA, une recherche pluridisciplinaire du Pasteur Network portant sur le retard de croissance et l’entéropathie environnementale pédiatrique. Il obtient son master en septembre 2017 et soutient sa thèse de doctorat en janvier 2023, sous la direction du Pr Marc-Éric Gruénais (université de Bordeaux) et du Dr Tamara Giles-Vernick (Institut Pasteur). Il dévoile les mécanismes généraux à l’origine de la situation des quartiers défavorisés d’Antananarivo et l’incapacité de leurs habitants à gérer les ordures ménagères, en s’appuyant sur l’Histoire, les sciences politiques et la géographie. Au lieu de tenter d’expliquer la malnutrition et le retard de croissance des enfants, il apporte des solutions pour les éviter. Depuis 2018, il est responsable adjoint de l’équipe « Santé et sciences sociales » de l’IPM.
- Amina GIHBID
Professeure adjointe des Instituts supérieurs des professions infirmières et techniques de santé (ISPITS), Maroc
Membre associée du laboratoire d’onco-virologie de l’Institut Pasteur du Maroc
Thèse : « Evaluation of viral, genetic and metabolic prognosis biomarkers for Nasopharyngeal cancer »
« […] et qu’en vérité, l’homme n’obtient que [le fruit] de ses efforts (39) et que son effort, en vérité, lui sera présenté (le jour du Jugement) (40). Ensuite il en sera récompensé pleinement » Sourate An-Najm (L’étoile), Coran

Titulaire d’un doctorat en virologie et biologie moléculaire, Amina Gihbid a mené ses recherches doctorales au sein du laboratoire d’onco-virologie de l’Institut Pasteur du Maroc (IPM) et de la faculté des sciences Aïn Chock de Casablanca (Maroc). Son travail portait principalement sur l’évaluation et l’identification de biomarqueurs viraux, génétiques et métaboliques potentiels, susceptibles de prédire les résultats du traitement précoce de patients atteints de carcinome nasopharyngé (NPC) et d’améliorer le pronostic de cette tumeur maligne particulièrement fréquente au Maroc. Il a permis d’établir que la charge virale de l’ADN du virus d’Epstein-Barr (EBV) circulant et certains paramètres métaboliques tirés d’un PET/CT au [18F] FDG constituaient des biomarqueurs pronostiques prometteurs dans la prise en charge clinique du NPC. Ces biomarqueurs pourraient ainsi contribuer à la personnalisation du traitement des patients en fonction du risque de rechute et de récidive.
À l’IPM, Amina Gihbid participe actuellement à deux projets, l’un s’intéressant à la « caractérisation de l’architecture épidémio-génétique du cancer du sein en Afrique du Nord : impact thérapeutique et socio-économique », et l’autre, à la médecine de précision en Afrique du Nord (PerMediNA). Dans le laboratoire d’onco-virologie de l’IPM, elle étudie également l’étiologie virale du carcinome oropharyngé et du cancer du sein au Maroc.

Activités transversales en génomique appliquée à Sciensano, Belgique
Thèse : « Exploring the added value of Whole Genome Sequencing in routine and pandemic viral surveillance »
« L’essence d’un doctorat réussi réside dans la capacité à évoluer et à adapter la recherche à un monde en constante mutation. »
Laura Van Poelvoorde a obtenu son master en sciences de l’ingénieur industriel, orientation biochimie, à l’université de Gand en 2017. Son intérêt pour la recherche et la santé publique l’a conduite à l’Institut scientifique de santé publique (WIV-ISP, désormais intégré à Sciensano), où elle a réalisé ses recherches doctorales dans le service « Activités transversales en génomique appliquée », sous la supervision de Nancy Roosens (Sciensano) et de Xavier Saelens (université de Gand). Ses recherches portaient sur des stratégies innovantes d’amélioration de la surveillance de la grippe, ce qui l’a amenée à explorer le séquençage de génome complet et son analyse. Cette expérience a été étendue au SARS-CoV-2 dans le cadre de la surveillance des eaux usées. Ce travail lui a permis de décrocher un doctorat en biochimie et biotechnologie en janvier 2023 et de publier 10 articles évalués par des pairs sur des stratégies génomiques contribuant à faire progresser la surveillance des virus respiratoires, au service de la société. Une fois diplômée, Laura Van Poelvoorde a accepté un poste permanent chez Sciensano, s’intéressant au développement de méthodes de détection de pathogènes dans les eaux usées.
- Irini THANOU
Laboratoire de cellules souches et de neuroimagerie / Département de neurobiologie, Institut Pasteur Hellénique, Grèce
Thèse : « Exploring the Brain’s Response to Chemotherapy: Neurogenesis at the Forefront »
« Déjà essayé. Déjà échoué. Peu importe. Essaie encore. Échoue encore. Échoue mieux. » S. Beckett

Le parcours académique d’Irini Thanou en neurobiologie s’est axé sur la compréhension de la dynamique complexe des niches neurogéniques adultes, tant dans l’homéostasie que dans la pathologie. Au cours de ses recherches doctorales, elle a découvert de nouvelles voies de migration des progéniteurs neuronaux en réponse à des agents chimiothérapeutiques, levant le voile sur l’interaction dynamique entre l’instinct et les signaux extrinsèques qui régulent les régions neurogéniques et les parenchymes cérébraux adjacents. En explorant la capacité de régénération du cerveau en réponse à la pathologie, elle a notamment contribué à la publication d’un projet utilisant des micro-ARN neurogéniques et de petites molécules pour la reprogrammation directe des astrocytes en neurones fonctionnels. L’Institut Pasteur a joué un rôle clé dans l’élaboration de ses recherches. Les collaborations au sein du réseau lui ont permis de participer à des projets portant sur les facteurs de risque de la maladie d’Alzheimer dans l’homéostasie cérébrale, qui ont apporté de précieux éclairages sur le rôle émergent de la neuroinflammation en tant que facteur déterminant de cette maladie. Elle a également coopéré activement à une étude sur les interactions dynamiques entre les astrocytes et la microglie pendant la neuroinflammation, en exploitant des techniques d’imagerie cérébrale intra-vitale de pointe. Elle aspire à ce que son prochain chapitre scientifique soit encore plus captivant.
- Beatriz CHAVES

Chercheuse en DTI (Conselho Nacional de Desenvolvimento Científico e Tecnológico, CNPq), Fondation Oswaldo Cruz (Fiocruz), Laboratoire de recherche sur le thymus (LPT)
Thèse : « Anti-VLA-4 antibodies for multiple sclerosis treatment: rational design and study of their mechanisms of action by high-content cell imaging »
« Relever des défis me fait me sentir vivante. »
Beatriz Chaves est une biotechnologue qualifiée en biologie des cellules T et développement des anticorps. Elle est titulaire d’un diplôme en biotechnologie (UFC, Fortaleza, Brésil), d’un master en biologie cellulaire et moléculaire (Fiocruz, Rio de Janeiro, Brésil) et d’un doctorat en biotechnologie et santé / biologie computationnelle et systémique (Fiocruz/INFINITy-INSERM, Eusébio/Rio de Janeiro/Toulouse, Brésil/France). Au cours de son parcours académique, elle a travaillé sur la conception, la production et l’évaluation fonctionnelle in silico d’anticorps ciblant l’antigène-4 d’activation très tardive (VLA-4) dans le traitement de la sclérose en plaques (SEP). Son doctorat l’a amenée à étudier, grâce à l’imagerie cellulaire à haut contenu, le profilage morphologique des lymphocytes des patients atteints de SEP afin de déterminer leur réponse clinique à la thérapie anti-VLA-4 actuelle à base d’anticorps. Les recherches, les collaborations et les compétences scientifiques développées par Beatriz Chaves tout au long de son cursus ont d’ores et déjà débouché sur un brevet, cinq articles publiés, un article accepté et deux articles en cours, ainsi que sur trois récompenses décernées lors de congrès. À présent, Beatriz Chaves a notamment pour objectifs de recherche une meilleure compréhension du rôle des cellules T dans la pathogenèse de la SEP et l’amélioration des immunothérapies des maladies chroniques actuelles.
- Noé OCHIDA
Institut Pasteur de Nouvelle-Calédonie
Institut Pasteur de Paris, unité Modélisation mathématique des maladies infectieuses
Thèse : « Modeling the dynamics of COVID-19, dengue, and the establishment of Wolbachia in Aedes aegypti populations in New Caledonia / Theme: Infectious diseases modeling »
« Une formidable aventure jalonnée de pas mal de rebondissements et de nombreuses joies. »

Originaire de Nouvelle-Calédonie, Noé Ochida a obtenu une licence en microbiologie à l’Université de Montpellier. Pour son master, il est passé de l’échelle microscopique à l’étude de l’écologie des maladies infectieuses. Conscient de l’impact de la dengue en Nouvelle-Calédonie, il a effectué son stage de M2 à l’Institut Pasteur de Nouvelle-Calédonie (IPNC) afin de travailler sur un enjeu de santé publique dans son île natale. Cette opportunité l’a conduit à réaliser un doctorat à l’IPNC, en collaboration avec l’IRD, sur la modélisation de la dynamique de la dengue et l’établissement de Wolbachia dans les populations d’Aedes aegypti en Nouvelle-Calédonie. Ses recherches portaient sur le risque climatique actuel et futur d’une épidémie de dengue en Nouvelle-Calédonie et exploitaient des projections climatiques à échelle réduite de modèles climatiques mondiaux. Noé Ochida a également modélisé le déploiement de la stratégie Wolbachia à Nouméa, suggérant des solutions optimales de mise en œuvre et évaluant son impact sur la transmission de la dengue. Il a eu l’opportunité d’apporter une aide à la modélisation aux décideurs lors de la crise de la COVID-19 en Nouvelle-Calédonie. Il effectue actuellement des recherches post-doctorales dans l’unité Modélisation mathématique des maladies infectieuses du Prof. Simon Cauchemez, à l’Institut Pasteur de Paris.
Lors de la réunion annuelle du Pasteur Network du 19 au 21 novembre 2023 à Tunis, le Dr. Ngu Abanda, du Centre Pasteur au Cameroun, a reçu le Prix Talent Pasteur Network 2023 décerné par le Président de l’Institut Pasteur, Stewart Cole. Les Talent Awards soutiennent le développement de carrière des jeunes scientifiques pour devenir de futurs leaders au sein du Réseau Pasteur.
Le Dr Ngu Abanda a obtenu son doctorat en médecine tropicale de l’Université d’Hawaï en 2017. Au cours de ses études de doctorat, il a mené des recherches sur les facteurs contribuant aux mauvais résultats du traitement chez les patients atteints de tuberculose, en particulier les enfants. Il a également évalué la précision de nouveaux tests moléculaires rapides pour le diagnostic de la tuberculose pharmacorésistante.
Après son doctorat, le Dr Ngu Abanda a choisi d’élargir ses connaissances sur le diagnostic clinique des maladies infectieuses et a pris le poste de microbiologiste au Laboratoire de santé publique du Département d’État des services de santé du Texas. Dans ce laboratoire, il a aidé à mettre en place un nouveau test moléculaire pour détecter Candida auris, un pathogène fongique émergent associé aux infections nosocomiales et considéré comme une menace grave pour la santé mondiale. Au cours de cette période postdoctorale, il a acquis une solide expérience dans le diagnostic clinique des maladies infectieuses. Il a rejoint le Centre Pasteur du Cameroun (CPC) en 2020, d’abord en tant que scientifique de laboratoire temporaire avec activité principale pour diriger une équipe travaillant 24 heures / 7 jours sur le diagnostic du COVID-19.
“Le Dr Ngu Abanda a apporté une contribution importante aux activités de diagnostic de la COVID-19 de la SCP et est devenu chercheur scientifique au CPC avec pour mission principale de développer des activités de recherche sur l’arbovirus. Il dirige aujourd’hui le laboratoire régional de référence (RRL) de la fièvre jaune de l’OMS et le laboratoire d’arbovirologie du CPC“, explique Mirdad Kazanji, directeur du Centre Pasteur du Cameroun.
Ses activités de recherche actuelles portent sur l’immunité à long terme du vaccin contre la fièvre jaune et la surveillance épidémiologique et entomologique des arbovirus.
“Fournir un diagnostic abordable et de qualité assuré pour éclairer les programmes de contrôle et de prévention des maladies à transmission vectorielle est le principe central de nos activités.” Dr Ngu Abanda
Son objectif à long terme est de développer un programme complet et multidisciplinaire de recherche et de formation sur les arbovirus grâce à son investissement quotidien aux côtés des équipes du CPC.
“Onze brillants jeunes scientifiques du Réseau Pasteur ont déjà reçu ce prix et continuent de contribuer de manière excellente à l’excellence scientifique du Réseau Pasteur. Aujourd’hui, nous sommes honorés de récompenser la qualité des premières réalisations du Dr Ngu Abanda et de soutenir sa carrière et ses développements ambitieux”, a souligné Stewart Cole, président de la Fondation Pasteur Network et président de l’Institut Pasteur.


Replay de la cérémonie d’ouverture :
A propos du Centre Pasteur du Cameroun
https://www.pasteur-yaounde.org/index.php/fr/
Consulter le Booklet de l’événement
A*STAR ID Labs – l’Agence singapourienne pour la science, la technologie et la recherche – Infectious Diseases Labs – et l’Institut Pasteur ont organisé conjointement un symposium impliquant le Pasteur Network.
Une délégation singapourienne d’A*STAR ID Labs était présente sur le campus de l’Institut Pasteur les 5 et 6 octobre 2023, dont la directrice exécutive d’A*STAR ID Labs, Prof Lisa Ng, et la directrice adjointe d’A*STAR ID Labs, Ms Amanda Loo. Lors de la séance d’ouverture, Son Excellence Mme FOO Teow Lee, Ambassadrice de Singapour en France, a réaffirmé la volonté de Singapour de favoriser les collaborations de recherche avec la France, et s’est félicitée du renforcement des liens entre A*STAR ID Labs et l’Institut Pasteur.
Un dialogue entre A*STAR et le Pasteur Network a été lancé grâce à la participation d’intervenants du réseau provenant de l’Institut Pasteur, de l’Institut Pasteur de Lille, de l’Institut Pasteur Corée, de l’Institut Pasteur du Cambodge et de l’Institut Pasteur de Nouvelle-Calédonie. Le Dr Rebecca F. Grais, directeur exécutive du Pasteur Network, a prononcé un discours d’ouverture sur le Pasteur Network, qui dispose d’un vaste réseau de recherche, de santé publique et d’épidémiologie.

Les présentations scientifiques se sont articulées autour de trois grands domaines de recherche : les maladies respiratoires, les maladies à transmission vectorielle et la résistance antimicrobienne. Ces domaines de recherche constituent des priorités scientifiques pour les laboratoires A*STAR ID et l’Institut Pasteur, ainsi que pour le Pasteur Network.
La première session a donné aux participants un aperçu des recherches en cours sur la tuberculose au sein du Pasteur Network et de l’Institut Pasteur, ainsi que sur la préparation aux épidémies au sein des laboratoires A*STAR ID. La deuxième session s’est concentrée sur les maladies à transmission vectorielle avec un large éventail de sujets abordés, tels que les interactions moustique-virus, la recherche sur les trypanosomes, et la dynamique virale-neuro-immune dans les infections à arbovirus, entre autres. La dernière session du symposium a présenté les dernières recherches sur la résistance aux antimicrobiens menées dans les laboratoires A*STAR ID, notamment sur la thérapie par les phages, à l’Institut Pasteur, par exemple sur le développement de nouveaux antibiotiques, et au sein du réseau Pasteur, sur la lutte en cours contre la résistance aux antibiotiques.
Environ cinquante pasteuriens ont participé aux sessions du symposium. Les présentations des orateurs ainsi que des moments d’échanges ont permis aux participants de discuter de futurs projets de recherche et de collaborations.









À propos de A*Star / ID Labs
Fondé en avril 2021 au sein de A*STAR (Agency for Science, Technology And Research), la principale agence publique singapourienne pour la R&D, ID Labs rassemble des chercheurs multidisciplinaires du monde entier œuvrant à l’obtention d’avancées en matière de préparation et de défense contre les menaces de maladies infectieuses émergentes, une vision partagée par l’Institut Pasteur et le Pasteur Network.
À propos du Pasteur Network
Vaste communauté humaine et scientifique, le Pasteur Network rassemble plus de 30 membres établis dans une vingtaine de pays qui contribuent ensemble à l’amélioration de la santé mondiale. Le réseau, au cœur de zones endémiques, dispose d’un accès privilégié à de très nombreux pathogènes qu’il surveille et étudie sur les 5 continents. Cette exceptionnelle diversité fait du Pasteur Network un acteur mondial unique de la santé publique, de la science, de l’innovation et de la formation, en particulier dans la lutte contre les maladies infectieuses.
Consult the Booklet of the event
A*STAR ID Labs – the Singapore Agency for Science, Technology and Research – Infectious Diseases Labs- and the Institut Pasteur have jointly organized a symposium involving the Pasteur Network.
A Singaporean delegation from A*STAR ID Labs was present at the Institut Pasteur campus on October 5 and 6, 2023, including A*STAR ID Labs Executive Director, Prof Lisa Ng, and A*STAR ID Labs Deputy Director, Ms Amanda Loo. On the opening session, Her Excellency Ms FOO Teow Lee, Ambassador of Singapore in France, reaffirmed the will of Singapore to foster research collaborations with France, and warmly welcomed the strengthening of ties between A*STAR ID Labs and the Institut Pasteur.

The scientific presentations were structured around three broad research areas: respiratory diseases, vector-borne diseases and antimicrobial resistance. Those research areas constitute scientific priorities for A*STAR ID Labs and the Institut Pasteur, as well as for the Pasteur Network.
The first session provided participants with an outline on ongoing tuberculosis research in the Pasteur Network and at the Institut Pasteur, and on epidemic preparedness at A*STAR ID Labs. The second session focused on vector-borne diseases with a wide-range of topics addressed, such as mosquito-virus interactions, trypanosome research, and viral-neuro-immune dynamics in arboviral infections, among others. The last session of the symposium outlined the latest research on antimicrobial resistance undertaken at A*STAR ID Labs, notably on phage therapy, at the Institut Pasteur, for instance on the development of new antibiotics, and in the Pasteur Network, regarding the ongoing battle against antibiotic resistance.
Around 50 colleagues from the Institut Pasteur campus attended the symposium sessions. The speakers’ presentations as well as more relaxed networking moments provided the participants with opportunities to discuss future research projects and collaborations.









About A*Star/ID Labs
Founded in April 2021 as part of the Agency for Science, Technology and Research (A*STAR), Singapore’s lead public sector R&D agency, ID Labs brings together a global and interdisciplinary team of scientists to generate purposeful outcomes towards preparedness and defense against emerging infectious disease threats, a vision shared by the Institut Pasteur and the Pasteur Network.
About the Institut Pasteur
The Institut Pasteur, a non-profit foundation with recognized charitable status set up by Louis Pasteur in 1887, is today an internationally renowned center for biomedical research. In the pursuit of its mission to tackle diseases in France and throughout the world, the Institut Pasteur operates in four main areas: research, public health, training, and development of research applications. The Institut Pasteur is a globally recognized leader in infectious diseases, microbiology, and immunology, with research focusing on the biology of living systems. Among its areas of investigation are emerging infectious diseases, antimicrobial resistance, certain cancers, neurodegenerative diseases, and brain connectivity disorders. The Institut Pasteur’s outstanding research is facilitated by the development of a technological environment of the highest standard, with core facilities for nanoimaging, computational biology and artificial intelligence. Since its inception, 10 Institut Pasteur scientists have been awarded the Nobel Prize for Medicine, including two in 2008 for the 1983 discovery of the human immunodeficiency virus (HIV) that causes AIDS. The Institut Pasteur is part of the Pasteur Network.
About the Pasteur Network
The Pasteur Network is a vast human and scientific community with more than 30 members in over 20 countries contributing together to global health. Located in the heart of endemic areas, the Network has privileged access to a large number of pathogens that it monitors and studies on all five continents. This exceptional diversity makes the Pasteur Network a unique global actor in public health, science, innovation, and education, especially in the fight against infectious diseases.
Pasteur Network annonce la mise en ligne du rapport qui porte sur les activités 2021-2022.
Ce dernier rapport regroupe une présentation du réseau et des faits marquants au niveau mondial concernant ses membres, ses réalisations et sa communauté.
Chacun des quatre chapitres est consacré à une région du Pasteur Network : Afrique, Amériques, Asie-Pacifique et Euro-Méditerranée avec une page spécifique pour chaque membre
Consulter le rapport 2021-2022
A propos du Pasteur Network
Vaste communauté humaine et scientifique, le Pasteur Network rassemble plus de 30 membres établis dans une vingtaine de pays qui contribuent ensemble à l’amélioration de la santé mondiale. Le réseau, au cœur de zones endémiques, dispose d’un accès privilégié à de très nombreux pathogènes qu’il surveille et étudie sur les 5 continents. Cette exceptionnelle diversité fait du Pasteur Network un acteur mondial unique de la santé publique, de la science, de l’innovation et de la formation, en particulier dans la lutte contre les maladies infectieuses.